Étape 1: Coefficients par rapport aux indices

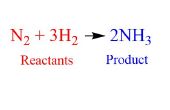
Lorsque vous approchez d’une équation chimique, il est important que vous compreniez la différence entre les coefficients et les indices. Le coefficient est placé en face d’une molécule, tandis que l’indice suit certains atomes comme le montre la première photo.
Dans une molécule, le coefficient correspond à la fraction de cette molécule présente. L’indice d’un atome indique la quantité de cet atome dans la molécule. Par exemple, dans la première photo le coefficient pour le second mandat indique que 3 molécules de H2 sont présents, et l’indice du premier terme signifie que 2 atomes d’azote (N) sont présents par molécule de N2.
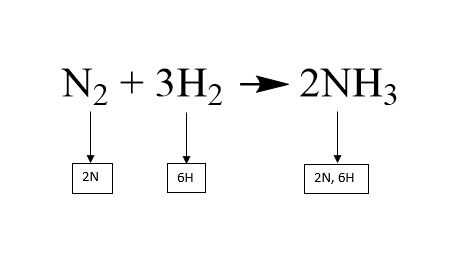
Ajout d’un coefficient devant une molécule multiplie tous les atomes au sein de cette molécule par le nombre du coefficient. Si un atome a un indice, le coefficient et l’indice se multiplient pour obtenir le montant total de l’atome dans la molécule. Par exemple, dans la deuxième photo, le coefficient pour l’ammoniac (NH3) du côté des produits est 2. Le 2 est multiplié par l’indice de l’hydrogène qui est 3, ce qui donne un nombre total d’atomes d’hydrogène égales à 6.
Le coefficient est la partie qui peut être modifiée et ajoutée lors de l’équilibrage d’une équation. Le coefficient de la modification du nombre total de cette molécule. L’indice, mais ne peuvent pas être modifié. Modifier un indice changerait la molécule elle-même.