Étape 1: Électrolyse de l’eau - une explication
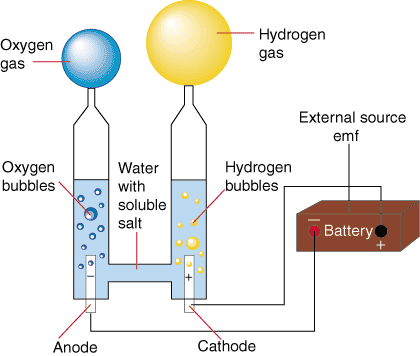
2H2O(l) = 2H2(g) + O2(g)
Comme chacun le sait, une molécule d’eau est formée par deux éléments : deux ions d’hydrogène positif et un ion négatif de l’oxygène. La molécule d’eau est maintenue par l’attraction électromagnétique entre ces ions. Quelle électricité est introduite dans l’eau par deux électrodes, une cathode (négative) et une anode (positive), ces ions sont attirés par l’électrode de charge opposée. C’est pourquoi les ions hydrogène chargées positivement recueillera sur la cathode et recueille l’oxygène chargée négativement sur l’anode.
Lorsque ces ions entrent en contact avec leurs électrodes respectives ils gagner ou perdent des électrons selon la charge ionique là. (Dans ce cas l’hydrogène gagne des électrons et l’oxygène perd eux) Faisant donc ces ions équilibrer leurs accusations et deviennent réels, électriquement équilibrées, atomes de bonne foi (ou dans le cas de l’hydrogène, une molécule).
Ce système n’est pas très efficace est parce que la partie de l’énergie électrique est convertie en chaleur au cours du processus. Il y a eu des rapports de rendement de 50 % - 70 %, mais je doute que c’est possible dans un environnement domestique. De toute façon, assez avec les trucs ennuyeux, permet d’aller effectuer certains gaz !