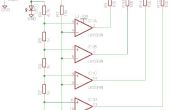
Étape 2: Composants : Graphite, dioxyde de titane, oxyde de Mangesium, HCl, chlorure d’aluminium et de l’urée





La batterie d’origine est une solution de l’AlCl, eau, Hcl, en aluminium et graphite. Cela a fonctionné, mais beaucoup souffert de l’auto-décharge, en quelques minutes. Il a montré la promesse, mais il a disparu trop vite. Après beaucoup d’expérimentation, j’ai découvert que le TiO2 et MgO a donné la batterie une « profondeur » de charge, probablement en raison de l’électrodéposition de métaux au sein de l’électrolyte... plus tard dans la section « Théorie de fonctionnement ».
Graphite - fantaisie ou simple, le graphite est graphite. Ma cellule de base utilisé en fait un morceau de bloc en forme de graphite d’artistes, vous pouvez utiliser tout ce qui - même portemine conduit... tout le chemin à des blocs de graphite coûteux ou des blocs de charbon actif. Le carbone est votre ami.
Poudre de dioxyde de titane est utilisé dans la peinture blanche, colorant alimentaire et toutes sortes de produits ménagers. Il est, comme la plupart des usages autour de la maison sont concernés, inerte. Je mine provenant d’une entreprise de fourniture de poterie en ligne. Vous pourriez facilement le trouver dans grands sacs de fournisseurs de gâteau ou de la fabrication du savon. Trucs polyvalent.
Oxyde de magnésium est utilisé comme un antiacide, devenant l’hydroxyde de magnésium lorsqu’il est mélangé avec de l’eau. C’est un peu caustique.
Notre objectif est de combiner ces avec HCl et facilitent leur réaction en TiCl et MgCl et demandez-leur de jouer avec l’AlCl comme notre électrolyte. Je ne suis pas sûr que cela se passe réellement dans la cellule de base jusqu'à ce que nous avons un solvant eutectiques profonds (plus tard) formé avec l’urée.
Chlorure d’aluminium est sorte de méchant. Porter des gants. Je n’a pas acheté de mine, mais fait en dissolvant le papier d’aluminium en HCl dilué. L’étape suivante détaille comment je l’ai fait, et pourquoi il était stupide de le faire à l’intérieur. Si vous achetez AlCl anhydre, savez que vous devez être très prudent de ne pas se répandre il et de porter un masque - c’est très mauvais pour vos poumons.
L’eau : Toute eau supplémentaire devra éventuellement être électrolysée dehors avant que la batterie viendra à plein potentiel. un peu d’eau est nécessaire pour ralentir la réaction de l’AlCl si vous rendre vous-même... donc il faut juste plus de temps à la condition de la batterie.
L’acide chlorhydrique est choses désagréables. Soyez prudent avec lui. J’ai acheté 200 compte-gouttes oculaire en plastique pour mesurer et distribuer. Il réagit avec l’eau dans l’air, dans votre nez, votre gorge et les poumons. La ventilation est votre ami. J’ai acheté l’acide à mon magasin local de matériel, généralement utilisé pour le nettoyage des briques ou en béton comme « Acide muriatique »
L’urée est un composant principal de l’urine. Je n’utilise pas d’urine. J’ai utilisé un tartinable "déglaçant" qui se compose principalement de l’urée. En outre, il a une couleur joli bleue. Certains centres de jardinage peuvent également vendre urée comme engrais. C’est le donateur de liaisons hydrogènes pour nos DES. Il s’agissait d’une addition postérieure dans ma pile de travail original, mais je vais l’ajouter dès le départ lors de l’électrolyte pour celui-ci. Les gants sont probablement une bonne idée.
MISE À JOUR 09/09/2015
Borax (Tétra du Borate de sodium) est un adoucisseur d’eau qui peuvent être acheté dans votre allée de lessive, il aussi fonctionne comme un flux pour le soudage et semble aider le maintien de l’alimentation et sortie des capacités de la batterie.
Encore une fois : La plupart des sel de trottoir sont juste sel, KCl ou NaCl - ce ne sont pas des substituts de l’urée. Si vous ne trouvez pas ce genre de choses (par exemple dans un climat chaud), regardez dans une jardinerie pour un engrais d’urée. Vous pouvez toujours faire vous-même, mais c’est une toute autre urine impliquant instructible.
Gants : Zut, juste porter des gants tout le temps - vous pouvez acheter une boîte de 50 pour quelques dollars.